
- Autor Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:14.
- Naposledy změněno 2025-01-22 15:56.
Informovaný souhlas je pokračující proces, který musí nastat dříve, než jakýkoli klinické hodnocení jsou prováděny související postupy. Proces se skládá z dokumentu a řady konverzací mezi klinické hodnocení účastník a hlavní zkoušející (PI) a delegovaní zdravotníci, podle potřeby.
Tímto způsobem, co je formulář informovaného souhlasu?
Hlavním zdrojem informací pro subjekty zvažující účast v klinických studiích je Formulář informovaného souhlasu (ICF). ICF je dokument, který vyžaduje podpis účastníka při účasti na klinické výzkumné studii. Klinický výzkum je komplexní předmět a dotýká se obtížné vědy.
jaké jsou 3 základní aspekty informovaného souhlasu a co znamenají? The tři základní principy Informovaný souhlas jsou: A. Dobrovolnost, Vyrovnanost, Respekt. B. Dobrovolnost, porozumění, zveřejnění.
Co je navíc informovaný souhlas v klinickém hodnocení?
The informovaný souhlas proces pro klinické testy má vám poskytovat průběžné informace, které vám pomohou učinit kvalifikované rozhodnutí, zda začít nebo zůstat v a klinické hodnocení . Osoba, která uvažuje o tom, že se stane součástí a klinické hodnocení se nazývá potenciál výzkum předmět.
Jaké jsou čtyři prvky informovaného souhlasu?
- Součásti informovaného souhlasu.
- Rozhodovací schopnost.
- Zveřejnění.
- Dokumentace souhlasu.
- Kompetence.
- Informovaný souhlas, právo odmítnout léčbu.
- Klinické zkoušky a výzkum.
Doporučuje:
Jaký je rozdíl mezi problémem řízení a problémem výzkumu?

Problém manažerského rozhodování se ptá, co musí DM udělat, zatímco problém marketingového výzkumu se ptá, jaké informace jsou potřeba a jak je lze nejlépe získat. Výzkum může poskytnout potřebné informace, aby se mohl správně rozhodnout. Problém rozhodnutí managementu je orientovaný na akci
Jaké jsou problémy marketingového výzkumu?
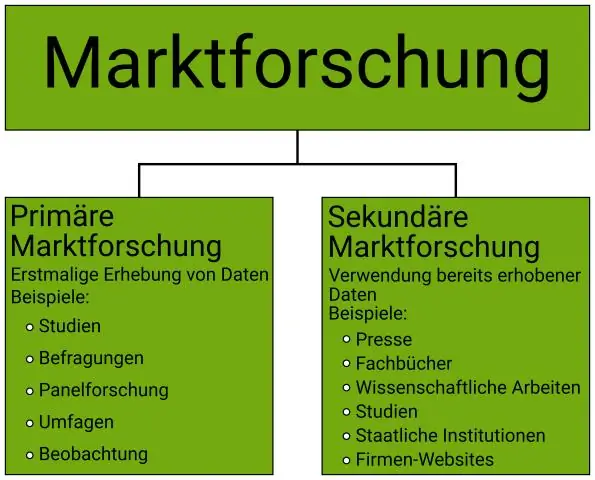
Při průzkumu trhu však dochází k několika běžným typům problémů, které mohou vést k příliš nákladným nákladům a mohou mít pro organizaci výsledky s diskutabilní hodnotou. Špatný design průzkumu. Neodpovídat na průzkum. Problém zaujatosti průzkumu. Problémy s pozorovacím výzkumem
Jaké je nejdůležitější využití marketingového výzkumu?

Objevte potenciální zákazníky a jejich potřeby, které lze začlenit do vašich služeb. Stanovte si dosažitelné cíle pro obchodní růst, prodej a nejnovější vývoj produktů. Dělejte dobře informovaná tržní rozhodnutí o svých službách a vyvíjejte účinné strategie
Jaké jsou nové trendy v obchodním výzkumu?

Pět rozvíjejících se trendů v oblasti Business Intelligence a Analytics Data Discovery urychluje samoobslužné BI a Analytics. Jednotný přístup a analýza všech typů informací zvyšuje produktivitu uživatelů. Velká data generovaná sociálními médii podporují inovace v zákaznické analýze. Textová analýza umožňuje organizacím interpretovat trendy sentimentu a komentáře v sociálních médiích
Může spoluvlastník provést převod bez souhlasu ostatních spoluvlastníků?

Spoluvlastník může svou část prodat nebo převést pouze tehdy, má-li k této části nemovitosti výhradní práva. Nemá-li výhradní práva každý spoluvlastník, nelze takový převod práv uskutečnit bez souhlasu ostatních spoluvlastníků
